导读:4月29日,关于瑞德西韦的疗效问题,来自中国的临床研究团队和吉利德、美国国家过敏和传染病研究所(NIAID)分别公布了三份结果。
但令人困惑的是,中国的临床试验没有显示出显著的效果,而吉利德和NIAID称其临床有效。
瑞德西韦到底有没有效果?
来 源丨21世纪经济报道(ID:jjbd21)
记 者丨卢杉
编 辑丨李一戈、张伟贤、刘巷
部分内容来源:澎湃新闻

图片来源 / 视觉中国
4月29日,顶尖医学杂志《柳叶刀》在线正式发表了瑞德西韦第一项临床试验的数据结果。
这是一项在中国湖北十家医院开展的,针对重症新冠肺炎(COVID-19)患者的随机、双盲、安慰剂对照的多中心试验。
简言之,这项临床试验结果显示,与安慰剂相比,接受瑞德西韦给药治疗并没有显著提高新冠肺炎患者的临床改善时间、死亡率或病毒清除时间。
换句话说,瑞德西韦的疗效不明显。
然而,美国的结果却截然不同。
同日,吉利德和美国国立卫生研究院(NIH)下属美国国家过敏和传染病研究所(NIAID)同时发布公告称其临床试验显示瑞德西韦显示出积极的效果,且已达到其主要终点。接受瑞德西韦治疗的晚期患者康复速度快于接受安慰剂的患者。
关于瑞德西韦
为何中美临床试验结论迥异?
据澎湃新闻报道,针对中美临床试验得出结论差异较大的疑问,瑞德西韦中国临床试验负责人曹彬教授回应记者称:
“这是两项不同的研究,评价标准不一样。”
曹彬教授向记者举例称,假设一个人身高1.75米,另一个人身高1.7499米,可以得出第一个人更高的结论吗?如果标准精确到1毫米,那第一个人就更高,如果1毫米忽略不计,那就两个人一样高。原因还是因为评价终点不一样。
“同样的高考分,你能上二本,上不了清华北大,标准不同。你说瑞德西韦有效吗,行,他能上大学,那也算是个好孩子,但是他上不了一本,就这么点事。”
曹彬对澎湃新闻记者举了个例子:
“一开始我们想象瑞德西韦是清华北大的苗子,但是实际上他上不了,家长对他要求太高了。”
据了解,此次中国团队进行的这项研究,是首个评估了静脉注射瑞德西韦对新冠肺炎成人重症住院患者有效性的随机、双盲、安慰剂对照临床试验。试验于湖北武汉的10家医院进行。研究在未达到预定的样本量的情况下终止。
4月29日晚,曹彬在接受澎湃新闻采访时曾表示,王辰院士全程指导参与了这项试验设计与进行,试验设计非常完善、在研究过程中执行了最严格的标准、实验结果可信度也是最高的。
英国爱丁堡大学的John Norrie教授(未参与该研究)在《柳叶刀》同期发表的述评文章中评价到:“这项研究设计合理,是一项双盲、安慰剂对照、多中心随机试验,并且实施良好,具有较高的方案依从性,且极少失访。”
关于中美试验方案差异,曹彬表示:美国NIH一开始用的标准和我们是一样的,它后来改了。
那么,中美的临床试验方案具体有何不同?
据第一财经报道,美国NIH和中国发表在《柳叶刀》的研究与设计均为双盲安慰剂对照临床(RCT),用药方案相同。“但是客观讲,中国瑞德西韦研究设计更加严格,科学性更强。”曹彬教授告诉第一财经记者。从主要终点来看,美国NIH设计的指标为临床恢复时间,中国则是设计了基于6分量表的临床改善时间。“NIH的恢复定义比较宽泛,包括住院,但不需要氧疗、出院(但可能仍有活动受限、需要吸氧),相当于我们的1-2级 回家吸氧。”曹彬教授表示。
中国科学报此前的一篇报道也提到,中国瑞德西韦重症临床试验入组率低与试验设计对患者入组条件严苛有关——两项临床试验分别要求患者在疾病确诊8天内和12天内没有接受过其他治疗。
对于这一设计,曹彬曾在公开场合多次表示,中国的两项瑞德西韦临床研究与美国NIH、WHO的试验设计相比,最大的差别就是在治疗窗口期方面用了非常严格的标准,而之所以这样设计,是因为他们发现在12天之内药物介入对于治疗新冠肺炎效果显著。
“美国NIH一开始用的标准和我们是一样的,它后来改了。”曹彬对澎湃新闻记者说。
目前,新冠肺炎还没有被证实有效的特效药。
《柳叶刀》:瑞德西韦治疗中国重症新冠肺炎患者无显著疗效
由于新冠肺炎至今没有特效药物,疫苗仍在路上,从1月末2月初开始的这场关于瑞德西韦有没有效果的讨论几乎周周上热门。回顾一下瑞德西韦“成名史”,结果还是要靠严格的临床试验数据说话。
瑞德西韦(Remdesivir)是一种核苷酸类似物,一开始是吉利德公司针对埃博拉病毒开发的,但它对埃博拉的作用不明显。由于在体外和体内动物模型中证明了对SARS和MERS等病毒病原体均有活性,研究人员推测它对于此次的新冠肺炎也有效。
瑞德西韦“成名史”
2020年1月19日,一名由武汉返美的35岁男子在华盛顿州确诊为新冠肺炎,后医生采用“同情用药”的方式对其注射了瑞德西韦,这名男子的临床状况得到大幅改善,瑞德西韦“一战成名”。
当时正是中国怡情焦灼的时期,中国的研究人员立即着手在武汉开展瑞德西韦针对新冠肺炎的临床试验。
2月2日,中日友好医院发布公告称:“中日友好医院在武汉疫区牵头开展瑞德西韦(Remdesivir)治疗2019-nCoV新型冠状病毒临床研究,为抗击怡情带来曙光。”
中日友好医院呼吸与危重症医学科主任曹彬团队在武汉发起了两项试验,根据ClinicalTrials.gov注册信息显示,针对重症和轻中症的两项试验注册日期分别为2月6日和2月5日。其时预期结束时间为4月底。
随着怡情在全球的扩散,瑞德西韦相继在美国和全球其他怡情严重的国家展开临床试验,其中既有研究者发起,也有吉利德自己发起的临床试验。
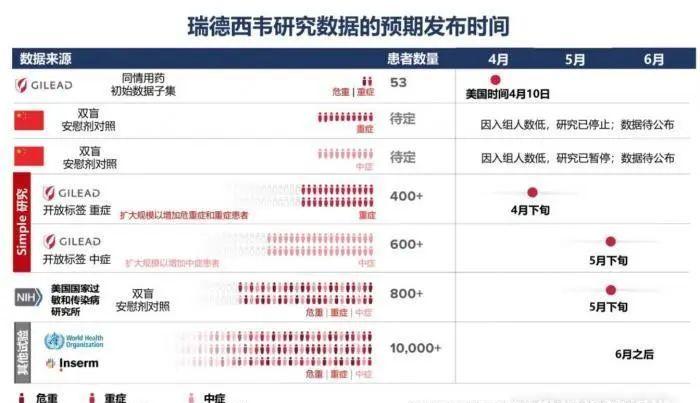
在全球翘首以盼瑞德西韦“揭盲”的时候,4月10日,针对瑞德西韦在全球的进展,吉利德科学董事长兼首席执行官Daniel O’Day发布了一封公开信,称目前瑞德西韦有七项临床试验已经启动,预计在4月底获得瑞德西韦针对重症患者研究的初步数据,但在中国“因入组停滞,针对重症患者的研究已停止。”
同时吉利德在《新英格兰医学杂志》上发布一项瑞德西韦(remdesivir)针对重症新冠病毒肺炎患者采用同情用药(compassionate use)的治疗结果。在接受同情使用瑞德西韦治疗的严重Covid-19住院患者中,在总共53例患者中,有36例(68%)观察到临床改善。但缺乏对照组试验,数据存在局限性。
4月15日,曹彬团队更新了这两项试验在全球最大的临床试验登记中心上的信息,重症状态更新为“终止”,轻中症状态更新为“暂停”,理由均为“COVID-19的流行在中国已经得到很好的控制,目前没有符合条件的患者可以被纳入。”
由于瑞德西韦被寄予厚望,吉利德市值在2020年一季度上涨14.5%,股价触及新高。

图片来源 / 澎湃新闻
戏剧性始于一周前的4月23日,由于世卫组织的一次“误操作”让中国临床试验结果提前意外曝光,称其疗效令人失望,本来走势良好的吉利德当天股价盘中突然跳水,一度下探超过8%,收跌4.34%。
这项试验即为此次《柳叶刀》发布的结果。
当天吉利德全球首席医疗官Merdad Parsey代表公司紧急发布声明称,“我们认为那篇文章包含了对研究的不恰当描述。由于入组率低,该研究被提前终止,因此,它的数据不足以支撑有统计意义的结论。”
一周后,《柳叶刀》发布了曹彬团队的“不尽如人意”的试验结果,而美国国立卫生院和吉利德坚持称瑞德西韦仍旧有效果。
根据吉利德发布的时间表,后续还有多项临床试验将公布结果。
中国临床试验结果
曹彬团队在中国湖北的十家医院进行了一项随机、双盲、安慰剂对照的多中心试验。
符合条件的患者是入院后经实验室确诊的SARS-CoV-2感染的成年人(≥18岁),从症状发作到入组间隔为12天或更短,室内空气或血液中氧饱和度不超过94%,动脉血氧分压与吸入氧分压不超过300 mm Hg的比率,以及放射学确定的肺炎。
而后随机将患者以2:1的比例随机分配给瑞德西韦静脉注射(第1天200 mg,然后在第2-10天100 mg,每日一次输注),或相同剂量的安慰剂输注10天。允许患者同时使用lopinavir–ritonavir,干扰素和皮质类固醇。
主要临床终点是随机分组后28天内达到临床改善的时间。临床改善被定义为按六点顺序量表将患者的入院状况降低两点,或从医院实时出院,以先到者为准。
六点量表如下:死亡= 6;体外膜氧合或机械通气入院= 5; 无创通气或高流量氧气疗法入院= 4;氧气治疗入院(但不需要大流量或无创通气)= 3;入院但不需要氧气治疗= 2; 并已出院或已达到出院标准(定义为临床恢复即发热正常,呼吸频率<每分钟24次呼吸,室内空气中的外周血氧饱和度> 94%,和咳嗽缓解,均维持至少72 h)= 1。
在2020年2月6日至2020年3月12日之间,筛选了255位患者,其中237位符合条件入组。158例患者接受了瑞德西韦治疗,79例接受了安慰剂治疗。安慰剂组中的一名患者在随机分组后撤回了先前书面知情同意书,因此意向治疗患者群(ITT)中包括158名和78名患者。
3月12日之后,由于武汉市爆发怡情得到控制,并且没有根据方案中指定的终止标准,因此没有患者入组。数据安全和监控委员会建议终止研究,并于3月29日对数据进行分析。
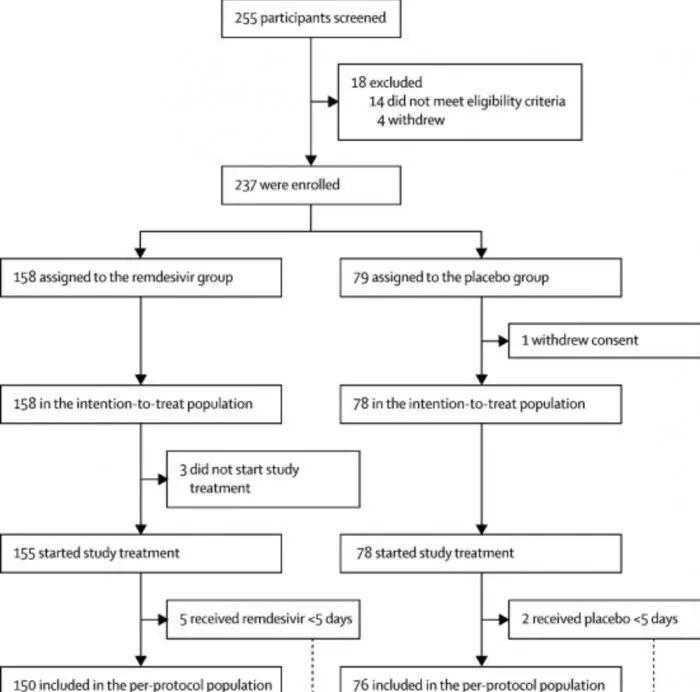
结果显示,使用瑞德西韦与改善临床疗效的时间无关(HR=1.23, 95% CI,0.87-1.75)。两组的28天死亡率相似(瑞德西韦组22例死亡[14%]安慰剂组为10(13%);差1·1%[95%CI -8·1至10·3])。
但在症状持续时间为10天或更短的患者中,接受瑞德西韦治疗的患者在临床上改善的时间要比接受安慰剂治疗的患者快得多(HR=1.52,95% CI,0.95-2.43)。
在155名接受瑞德西韦治疗的患者有102名(66%)发生不良事件,78名安慰剂接受者中有50名(64%)发生不良事件。瑞德西韦组最常见的不良反应是便秘,低白蛋白血症,低钾血症,贫血,血小板减少和总胆红素升高。在安慰剂组中,最常见的是低白蛋白血症,便秘,贫血,低钾血症,天冬氨酸转氨酶升高,血脂升高和总胆红素升高。
研究人员认为,在这项针对重度新冠患者住院的成年患者的研究中,瑞德西韦没有表现出统计学上显著的临床获益。然而,较早治疗者中临床改善时间的数量减少需要更大的研究证实。
尽管在冠状病毒感染的临床前模型中显示出强大的抗病毒作用,但在本研究中,瑞德西韦没有导致SARS-CoV-2 RNA载量或上呼吸道或痰标本的可检测性显著降低。
研究发现瑞德西韦具有足够的耐受性,未发现新的安全隐患。此外,对于重度新冠患者,更长的疗程和更高剂量的瑞德西韦是否有益,尚无答案。
吉利德和美国NIAID:
瑞德西韦临床试验显示出积极效果

图片来源 / 图虫创意
更具有戏剧性的是,4月29日,吉利德和美国国立卫生研究院(NIH)下属美国国家过敏和传染病研究所(NIAID)分别发公告称其所开展的瑞德西韦临床试验显示出积极效果。

吉利德披露信息
吉利德宣布的是一项开放标签的3期SIMPLE试验的主要结果,该试验评估了住院严重COVID-19疾病患者接受瑞德西韦5天和10天给药时间的结果:
瑞德西韦5天给药方案较10天给药方案显示出相似的临床改善。并且,越早接受瑞德西韦治疗的患者临床改善情况越好(发病10天内和10天后接受治疗的患者第14天出院比例分别为62%和49%)。
NIAID的研究则是一项涉及1063名患者的随机对照试验的初步数据分析,该试验从2月21日开始,接受瑞德西韦的新冠肺炎晚期住院患者的康复速度快于接受安慰剂的类似患者。
负责监督试验的独立数据和安全监视委员会(DSMB)于4月27日举行会议,以审查数据并与研究小组共享其中期分析结果。基于对数据的审查,他们指出,从主要终点、恢复时间(这是流感试验中常用的一种指标)的角度来看,瑞德西韦优于安慰剂。本研究中的恢复被定义为足以出院或恢复正常活动水平。
初步结果表明,接受瑞德西韦的患者的康复时间比接受安慰剂的患者快31%(p <0.001)。接受瑞德西韦治疗的患者的中位恢复时间为11天,而接受安慰剂的患者为15天。结果还显示了生存益处,接受瑞德西韦组的死亡率为8.0%,而安慰剂组的死亡率为11.6%(p = 0.059)。
受该消息提振,吉利德当日盘中大涨超过8%,市值过千亿美元。也有华尔街分析师认为,FDA可能会因此加速批准瑞德西韦上市。
瑞德西韦到底有没有效果?
吉利德CEO又发了一封公开信
关于瑞德西韦的疗效问题,来自中国的临床研究团队和吉利德、美国国家过敏和传染病研究所(NIAID)分别公布了三份结果。但令人困惑的是,中国的临床试验没有显示出显著的效果,而吉利德和NIAID称其临床有效。
4月30日,吉利德科学董事长兼首席执行官Daniel O’Day发布了一封公开信,涉及上述两项试验。
“在过去的两个月里,大家满怀期望,等待着用科学解读瑞德西韦(Remdesivir)。虽然在这一过程中有一些线索,但我们知道,只有临床试验才能为其是否可以安全有效地治疗新型冠状病毒肺炎提供答案。今天,我们获得了一些初步的答案。”
美国国家过敏和传染病研究所(NIAID)进行的全球性的、安慰剂对照试验的结果是积极的。结果表明,新型冠状病毒肺炎患者接受瑞德西韦治疗比接受安慰剂恢复得更快。
我们还有更多的工作要做,瑞德西韦尚未被批准,然而,对于这些积极的结果可能带给患者的意义,所有吉利德人都深感责任重大。经过了多年来对瑞德西韦的研究和努力,我们的团队今天感到欣慰和感激,我们的努力是如此值得。
早在我们知道新型冠状病毒肺炎暴发之前,这项工作就已经开始了。瑞德西韦是吉利德的科学家们十多年研究、反复试验和努力的结果。近年来,我们一直在研究其对于埃博拉病毒、马尔堡病毒和尼帕病毒等出血性病毒以及非典型性肺炎(SARS)病毒和中东呼吸综合征(MERS)等其他冠状病毒的作用。我们已经积累了充足的认知,所以,当新型冠状病毒出现时,我们可以很快进入临床试验。
自一月份以来,我们的团队夜以继日地工作,以确定瑞德西韦是否可以用于新型冠状病毒肺炎患者。这些努力包括与研究人员和各国政府就各种临床试验进行合作。今天的新闻中提到,瑞德西韦可能在减轻疾病大流行的负担方面发挥作用,这是我们都希望能出现的结果。
关于今天发布的结果
美国国家过敏和传染病研究所的研究是一系列临床试验的一部分,旨在研究瑞德西韦的有效性。在设计整体临床项目时,我们以这样一种方式来做,可以并行探索多个问题,包括哪些组的患者最有可能出现应答,何时开始治疗以及疗程持续多久。我们使用了各种研究设计,从安慰剂对照到开放标签,来回答每种情况下非常具体的问题。我们希望答案能在同一时间显现,通过汇总它们将清晰地显示出如何能使瑞德西韦最好地用于患者。
今天,除了美国国家过敏和传染病研究所关于有效性和安全性的数据,我们还获得了吉利德主导的针对新型冠状病毒肺炎重症患者治疗疗程的三期SIMPLE试验数据。关于疗程的问题至关重要,如有可能使用较短的疗程,我们将在很多方面获益:患者可以更早出院回家,家人可以团聚,医疗资源可以减负,更多的药物可以提供给其他有需要的患者。在疾病大流行时期,这些都尤其重要。
SIMPLE临床试验已经评估了瑞德西韦5日治疗疗程是否能达到和10日治疗疗程相似的结果。来自第一个研究的数据表明,对于新型冠状病毒肺炎重症患者而言,无论接受5日还是10日疗程,其临床改善是相似的。我们非常高兴看到这些结果。这提供了关于重症患者治疗疗程的非常有价值的信息,这也是我们一直以来希望看到的结果。
这样的结果对瑞德西韦的供应有着积极的影响。在耗时长且复杂的生产流程有各种限制的情况下,我们的团队自一月起已经开始加速生产。包括在等待分配的成品和处于最后生产阶段的制剂在内,我们现有的供应量共有150万剂。我们预估这些将可用于14万个10日疗程。如能将重症患者的疗程缩短,我们将可以显著提升吉利德已承诺捐赠的这些药物所覆盖的疗程数量。
基于美国国家过敏和传染病研究所的试验和SIMPLE研究的数据,我们可以知晓两点:瑞德西韦可以缩短患者的恢复时间;当治疗重症患者时,其5日疗程具有与10日疗程相似的有效性。
前进的道路
瑞德西韦的故事始终围绕着合作和科学,而这些也将持续引领我们未来的举措。
今天的结果,为接下来探索瑞德西韦的应用和潜力带来很多机会。我们的团队将研究其他的剂型和用药方法,探寻将此药物带给更广泛患者人群的方式。我们也将与合作伙伴一同研究瑞德西韦与其他疗法联合使用的可能性。
在供应方面,我们正在建立一个全球性的制药和化学制品生厂商联合网络,以扩大全球产能和产量。通过国际合作共同为全球患者提供充足的供应,这将是至关重要的,我们期待着这样的协同努力。在法规监管层面,我们正在和不同团体讨论如何将瑞德西韦提供给发展中国家。
感谢和瑞德西韦一起努力的每一个人:从参与临床试验的患者、医护人员、研究学者到很多其他的团体组织。我们深知,要找到终止疾病大流行的医学方案,还有很多的工作要做,有很长的路要走。与此同时,今天关于瑞德西韦的新闻代表着我们取得的重要进展,它在这个大众急切期待的时刻为我们点亮了希望。

本期编辑 刘巷、实习生华凯纯

瑞德西韦临床试验结果(临床试验的结果评价一般不使用)
编辑:昊阳