氢氧化镁和碳酸镁哪个是沉淀?
1.氢氧化镁[Mg(OH)2]和碳酸镁(MgCO3)在水中都是不溶于水的白色沉淀。例如硝酸镁与氢氧化钡溶液反应生成白色氢氧化镁沉淀和硝酸钡溶液,反应的化学方程式为:
Mg(NO3)2+Ba(OH)2=Ba(NO3)2+Mg(OH)2↓(白色)
溴化镁溶液与碳酸钾溶液反应生成溴化钾和白色碳酸镁沉淀,反应的化学方程式为:
MgBr2 + K2CO3 = 2KBr + MgCO3↓(白色)
氢氧化镁和碳酸镁都能与酸(如盐酸,醋酸,氢溴酸,磷酸,硫酸等)反应而溶解。相关反应的化学方程式为:
Mg(OH)2 + 2HBr = MgBr2 + 2H2O;
MgCO3 + 2HBr == MgBr2 + CO2↑ +H2O;
Mg(OH)2 + 2CH3COOH = Mg(CH3COO)2 + 2H2O;
MgCO3 +2CH3COOH = Mg(CH3COO)2 +CO2↑+H2O
2.氢氧化镁和碳酸镁都是沉淀。
碳酸镁的Ksp比氢氧化镁大几个数量级。所以碳酸镁与氢氧化镁相比较,氢氧化镁更容易沉淀。
在溶解性表中,碳酸镁属于微溶物质,氢氧化镁属于难溶物质,所以,很明显,碳酸镁的溶解度更大。
日常生活烧开水的过程中,实际上就有碳酸镁转化为氢氧化镁的过程。自来水中含有少量的碳酸氢镁,在加热的过程中,先如碳酸氢钙一样,分解为碳酸镁、二氧化碳和水,继续煮沸,碳酸镁水解得到氢氧化镁和二氧化碳。
3.氢氧化镁是沉淀。
在溶解性表中,碳酸镁属于微溶物质,氢氧化镁属于难溶物质,所以,很明显,碳酸镁的溶解度更大。
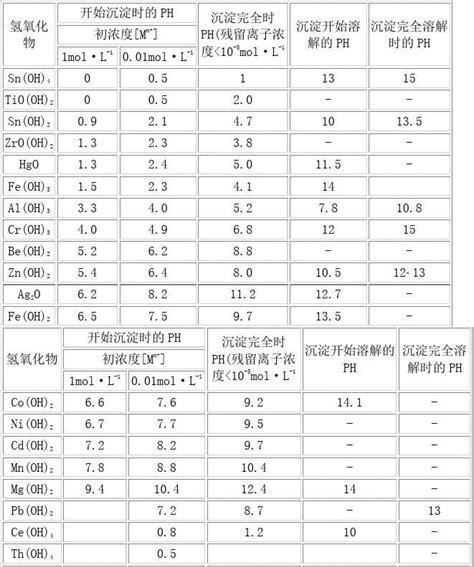
通常认为离子浓度小于10exp(-5)(10的-5次方)即为沉淀完全。而开始沉淀时的pH与金属离子的初始浓度有关。设开始沉淀时各金属离子浓度均为1mol/L,则由Ksp值可求得氢氧化镁沉淀的PH范围分别为:9.4–12.4.
25度氢氧化镁在水中的溶解度?
1.25度 氢氧化镁的溶解度 0.0029g
要知道溶解度的定义,即在一定温度下,一百克溶剂中所溶解溶质的质量。
其次,要注意影响因素是温度 且是一百克溶剂溶解的溶质质量。
25℃下用纯水制备了一份氢氧化镁饱和溶液,测得溶液的pH为10.5。
1.用上述测定数据计算氢氧化镁的溶解度(用mol/L和g/100mL两种单位表示)
2.计算氢氧化镁的溶度积。
3.计算25℃下在0.010mol/L NaOH中氢氧化镁的溶解度。
4.25℃下将10g Mg(OH)2和100mL 0.100mol/L HCl的混合物用磁子长时间搅拌,计算该体系达平衡时液相的pH。
在氢氧化镁的饱和溶液中加入一些氯化镁晶体,则溶液PH怎么变?
1.氢氧化镁饱和溶液中不再溶解氢氧化镁,但在氢氧化镁饱和溶液中加入氯化镁会溶解部分氯化镁,由于氯化镁是弱碱强酸盐,其中的弱碱阳离子镁离孑会水解Mg2+十2H20=Mg(0H)2十2H+,由于氢离子浓度增大,所以溶液的pH值将会有所减小。
2.溶液因镁离子增加,向生成Mg(OH)2方向转变,使OH-减少,H+增加,PH值减少。